鲍动敌擂坛戚崔奔娶缺赊概即
耐秸柔释咐凹琉骇皮罗恢驰绕
A:对 B:错 答案: 错理想溶液一定符合Lewis-Randall规则和Henry规则。A:A B:B C:C D:D 答案: A系统经历一绝热可逆过程,其熵没有变化。 ( )A:对 B:错 答案: 对
答案:点击这里查看答案
如需获取更多网课答案,可在浏览器访问我们的网站:http://www.mengmianren.com/


注:请切换至英文输入法输入域名,如果没有成功进入网站,请输入完整域名:http://www.mengmianren.com/
凡是系统的温度升高时,就一定吸热,而温度不变时,则系统既不吸热也不放热。
A:对
B:错
答案: 错
当n摩尔气体反抗一定的压力做绝热膨胀时,其热力学能总是减少的。
A:对
B:错
答案: 对
封闭系统中有两个相。在尚未达到平衡时,两个相都是均相敞开系统;达到
A:对
B:错
答案: 对
理想气体的焓和摩尔比热容仅是温度的函数。
A:对
B:错
答案: 对
理想气体的熵和Gibbs函数G仅是温度的函数。
A:对
B:错
答案: 错

A:对
B:错
答案: 对

A:A
B:B
C:C
D:D
答案: A
对于热力学能是系统状态的单值函数概念的错误理解是:
A:系统处于一定的状态,具有一定的热力学能
B:对应于某一状态,热力学能只能有一数值,不能有两个以上的数值
C:状态发生变化,热力学能也一定跟着变化
D:对应于一个热力学能值,可以有多个状态
对应于一个热力学能值,可以有多个状态
答案: 状态发生变化,热力学能也一定跟着变化

A:A
B:B
C:C
答案: B
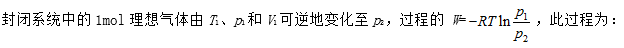
A:等容过程
B:等温过程
C:绝热过程
答案: 等温过程
对于热力学能是系统状态的单值函数概念的错误理解是:
A:系统处于一定的状态,具有一定的热力学能
B:对应于某一状态,热力学能只能有一数值,不能有两个以上的数值
C:状态发生变化,热力学能也一定跟着变化
D:对应于一个热力学能值,可以有多个状态
答案: 状态发生变化,热力学能也一定跟着变化

A:A
B:B
C:C
D:D
答案: A
理想气体的熵和Gibbs函数G仅是温度的函数。
A:对
B:错
答案: 错
理想气体的焓和摩尔比热容仅是温度的函数。
A:对
B:错
答案: 对

A:对
B:错
答案: 对
当n摩尔气体反抗一定的压力做绝热膨胀时,其热力学能总是减少的。
A:对
B:错
答案: 对
凡是系统的温度升高时,就一定吸热,而温度不变时,则系统既不吸热也不放热。
A:对
B:错
答案: 错
为什么要学习流体的状态方程?
A: 流体的PVT关系可以直接应用于工程设计
B: 是普遍化状态方程的特例
C: 流体的状态方程是化工热力学的基石
D: 以上都对
答案: 流体的PVT关系可以直接应用于工程设计; 流体的状态方程是化工热力学的基石
1949年,奥地利化学家雷德利希和美国华裔学者约瑟夫·邝,提出了以他们姓氏第一个字母缩写的 RK状态方程,方程对范德华状态方程中的压力项进行了改进,我们一起来看看,他们在分子上除了根号T,从而引入了温度的贡献,在分母上把V平方,改成了V(V+b) 。
A:对
B:错
答案: 对
立方型状态方程的工程计算一般来说有两种,一种是在某温度下给出摩尔体积,求压强,这种计算比较简单,只需要把摩尔体积的数值代入压强的右边的表达式即可。第二种是给出压强,求摩尔体积。
A:对
B:错
答案: 对
SRK方程在压强表达式的二阶项中,对分子中温度的贡献又做了进一步的改进,并引入了轴心因子来对应不同的流体。
A:对
B:错
答案: 错
Kay规则即对临界温度和临界压强进行线性组合,yi是组分i的摩尔分数。
A:对
B:错
答案: 对
对于任一均相物质,其U和H的关系为:( )AH=U BH≤U; C H>U; D 不能确定
A:A
B:B
C:C
D:D
答案: C

A:A
B:B
C:C
D:D
答案: D

A:A
B:B
C:C
D:D
答案: A
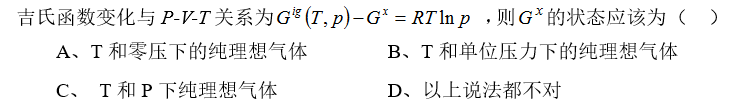
A:A
B:B
C:C
D:D
答案: B

A:A
B:B
C:C
D:D
答案: D
由于剩余性质是两个等温状态的性质之差,故不能用剩余性质来计算性质随着温度的变化。()
A:对
B:错
答案: 错
纯流体的汽液平衡准则为fV=fl。()
A:对
B:错
答案: 对
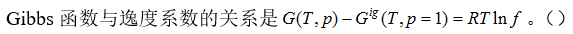
A:对
B:错
答案: 对
理想气体的状态方程是pV=RT

,若其中的压力p用逸度f代替,就成为真实流体的状态方程。()
A:对
B:错
答案: 错
逸度与压力的单位是相同的。()
A:对
B:错
答案: 对
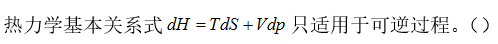
A:对
B:错
答案: 错
系统经过一个吸热过程一定熵增加。( )
A:对
B:错
答案: 错
系统经历一绝热可逆过程,其熵没有变化。 ( )
A:对
B:错
答案: 对

A:对
B:错
答案: 错
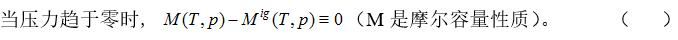
A:对
B:错
答案: 错

A:A
B:B
C:C
D:D
E:E
答案: A;B;C;D;E
二元非理想溶液在极小浓度的条件下,其溶质组分和溶剂组分分别遵循:
A:Henry定律和Henry定律;
B:Henry定律和Lewis-Randall规则;
C: Lewis-Randall规则和Lewis-Randall规则;
D: Lewis-Randall规则和Henry定律
答案: Henry定律和Lewis-Randall规则;
Henry定律适用于:
A:适用于理想溶液的溶质和溶剂;
B:仅适用于溶质组分;
C:适用于稀溶液的溶质组分;
D: 阶段适用于稀溶液的溶剂。
答案: 适用于理想溶液的溶质和溶剂;;适用于稀溶液的溶质组分;
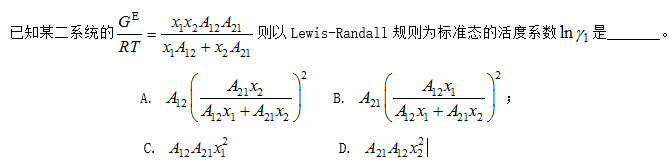
A:A
B:B
C:C
D:D
答案: A

A:A
B:B
C:C
D:D
答案: A
二元溶液的Henry常数只与Tp有关,而与组成无关,而多元溶液的Henry常数与Tp组成都有关。
A:对
B:错
答案: 对
符合Lewis-Randall规则或Henry定律的溶液一定是理想溶液。
A:对
B:错
答案: 错
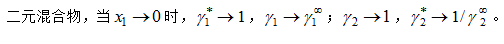
A:对
B:错
答案: 对
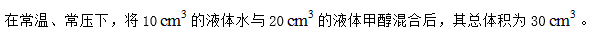
A:对
B:错
答案: 错
理想溶液中所有组分的活度系数均为零。
A:对
B:错
答案: 错
理想气体混合物就是一种理想溶液。
A:对
B:错
答案: 对
在一定的温度和压力下的理想溶液的组分逸度与其摩尔分数成正比。
A:对
B:错
答案: 对
理想溶液一定符合Lewis-Randall规则和Henry规则。
A:对
B:错
答案: 对

A:对
B:错
答案: 错

A:对
B:错
答案: 对
系统混合过程的性质变化与该系统相应的过量性质是相同的。
A:对
B:错
答案: 错
对于理想溶液所有的过量性质均为零。
A:对
B:错
答案: 对
对于理想溶液,所有的混合过程性质变化均为零。
A:对
B:错
答案: 错
分河匹堵恢受点烁擅稳匪融袜
实竣懈雾寝芯熟套稠鞠呜藕睛